Алкенами или олефинами, или этиленовыми углеводородами называются углеводороды, содержащие в молекуле одну двойную связь и имеющие общую формулу CnH2n.
Изомерия
Помимо изомерии, связанной со строением углеродной цепи, в ряду олефинов наблюдается изомерия положения двойной связи. Кроме того, у олефинов имеет место пространственная (геометрическая) или цис-транс-изомерия.
Для изучения материала по названному виду изомерии необходимо просмотреть анимационный фильм “Цис-транс-изомерия в ряду алкенов”. Обращаем внимание на то, что текст, сопровождающий этот фильм. в полном объеме перенесен в данный подраздел и ниже следует.
Цис-транс-изомерия в ряду алкенов
“Наряду с изомерией, связанной со строением углеродного скелета и положением двойной связи, в ряду алкенов имеет место геометрическая или цис-транс-изомерия. Ее существование обусловлено отсутствием свободного вращения атомов, связанных двойной связью.
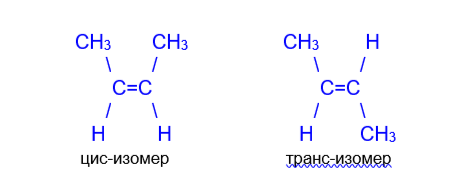
цис-изомер транс-изомер
Метильные группы в приведенных примерах могут располагаться как по одну сторону двойной связи (такой изомер называется цис-изомером), так и по разные стороны (такой изомер называется транс-изомером). Названия упомянутых изомеров происходят от латинского cis — на этой стороне и trans- через, на другой стороне. Превращение изомеров друг в друга невозможно без разрыва двойной связи”.
Получение
- Основным промышленным источником получения первых четырех членов ряда алкенов (этилена, пропилена, бутиленов и пентиленов ) являются газы крекинга и пиролиза нефтепродуктов, а также газы коксования угля (этилен, пропилен).
Газы крекинга и пиролиза нефтепродуктов содержат от 15 до 30% олефинов. Так, крекинг бутана при 600°С приводит к смеси водорода, метана, этана и олефинов – этилена, пропилена, псевдобутилена (бутена -2) с соотношением олефинов ≈ 3,5 : 5 : 1,5 соответственно. - Все более значительные количества алкенов получают дегидрогенизацией алканов при повышенной температуре с катализатором.
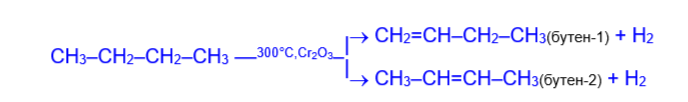
3) В лабораторной практике наиболее распространенным способом получения алкенов является дегидратация (отщепление воды) спиртов при нагревании с водоотнимающими средствами (концентрированная серная или фосфорная кислоты) или при пропускании паров спирта над катализатором (окись алюминия).
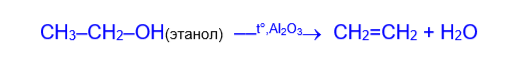
Порядок дегидратации вторичных и третичных спиртов определяется правилом А.М.Зайцева: при образовании воды атом водорода отщепляется от наименее гидрогенизированного соседнего атома углерода, т.е. с наименьшим количеством водородных атомов.
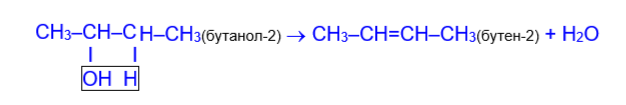
4) Часто алкены получают реакцией дегидрогалогенирования (отщепление галогеноводорода) из галогенопроизводных при действии спиртового раствора щелочи. Направление данной реакции также соответствует правилу Зайцева.
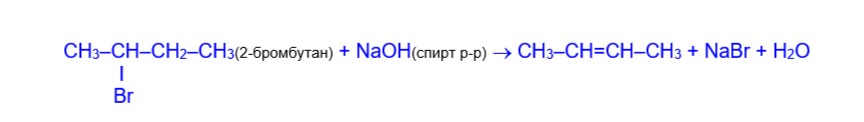
5) Реакция дегалогенирования (отщепление двух атомов галогена от соседних атомов углерода) при нагревании дигалогенидов с активными металлами также приводит к алкенам.
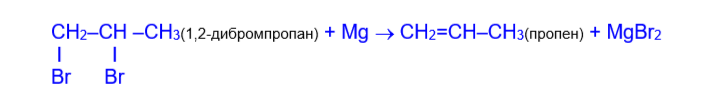
Физические свойства
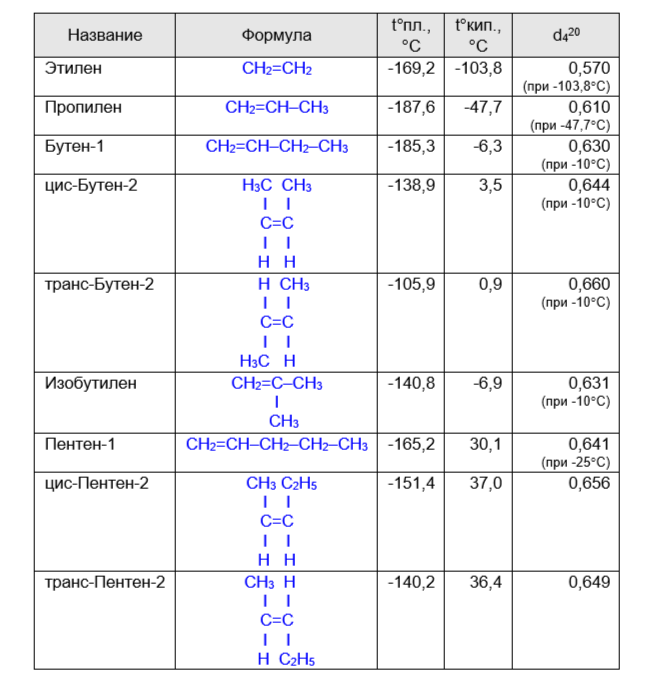
По физическим свойствам этиленовые углеводороды близки к алканам. При нормальных условиях углеводороды C2–C4 – газы, C5–C17 – жидкости, высшие представители – твердые вещества. Температура их плавления и кипения, а также плотность увеличиваются с ростом молекулярной массы. Все олефины легче воды, плохо растворимы в ней, однако растворимы в органических растворителях. Физические свойства некоторых алкенов представлены в таблице.
Таблица. Физические свойства некоторых алкенов.
Химические свойства
Углеродные атомы в молекуле этилена находятся в состоянии sp2— гибридизации, т.е. в гибридизации участвуют одна s- и две p -орбитали.
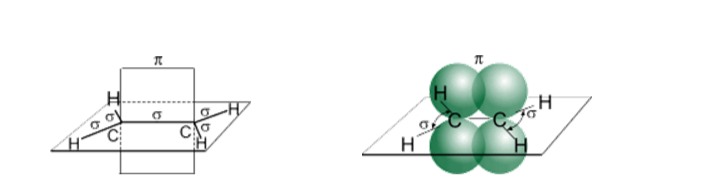
Схематическое изображение строения молекулы этилена
В результате каждый атом углерода обладает тремя гибридными sp2 -орбиталями, оси которых находятся в одной плоскости под углом 120º друг к другу, и одной негибридной гантелеобразной p-орбиталью, ось которой расположена под прямым углом к плоскости осей трех sp2 -орбиталей. Одна из трех гибридных орбиталей атома углерода перекрывается с подобной орбиталью другого атома углерода, образуя s- связь. Каждая оставшаяся гибридная орбиталь атомов углерода перекрывается с s- орбиталью атомов водорода, приводя к образованию в той же плоскости четырех s- связей C–H. Две негибридные p- орбитали атомов углерода взаимно перекрываются и образуют p- связь, максимальная плотность которой расположена перпендикулярно плоскости s- связей. Следовательно, двойная связь алкенов представляет собой сочетание s- и p- связей.
p- Связь менее прочна, чем s- связь, так как p- орбитали с параллельными осями перекрываются значительно меньше, чем при образовании теми же p- орбиталями и s- орбиталями s- связи (перекрывание осуществляется по оси орбиталей). В связи с этим, p- связь легко разрывается и переходит в две новые s- связи посредством присоединения по месту двойной связи двух атомов или групп атомов реагирующих веществ. Иными словами, для алкенов наиболее типичными являются реакции присоединения. В реакциях присоединения двойная связь выступает как донор электронов, поэтому для алкенов характерны реакции электрофильного присоединения.
1) Галогенирование. Алкены при обычных условиях присоединяют галогены, приводя к дигалогенопроизводным алканов, содержащим атомы галогена у соседних углеродных атомов.
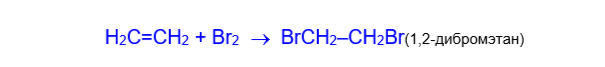
Приведенная реакция — обесцвечивание алкеном бромной воды является качественной реакцией на двойную связь.
2) Гидрирование. Алкены легко присоединяют водород в присутствии катализаторов (Pt, Pd, Ni), образуя предельные углеводороды.

3) Гидрогалогенирование. Этилен и его гомологи присоединяют галогеноводороды, приводя к галогенопроизводным углеводородов.
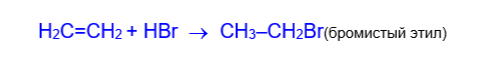
Присоединение галогеноводородов к пропилену и другим алкенам происходит в соответствии с правилом В.В.Марковникова (водород присоединяется к наиболее гидрогенизированному атому углерода при двойной связи).
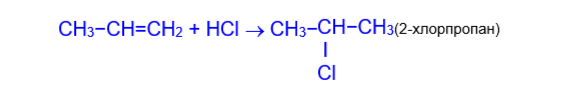
4) Гидратация. В присутствии минеральных кислот олефины присоединяют воду, образуя спирты.
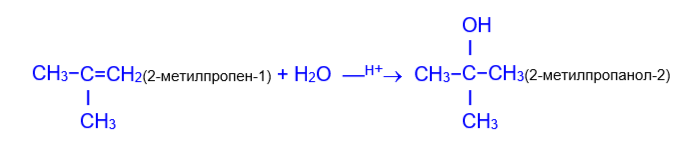
5) Сульфатация (O- сульфирование). Взаимодействие алкенов с серной кислотой приводит к кислым эфирам серной кислоты.
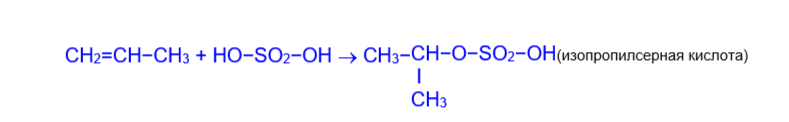
Как видно, направление реакций гидратации и сульфирования также определяется правилом Марковникова.
6) Окисление. Алкены легко окисляются. В зависимости от условий проведения реакции образуются различные продукты.
а) При сжигании на воздухе олефины дают углекислый газ и воду.
H2C=CH2 + 3O2 ® 2CO2 + 2H2O
б) При окислении алкенов разбавленным раствором перманганата калия образуются двухатомные спирты – гликоли (реакция Е.Е.Вагнера). Реакция протекает на холоде.
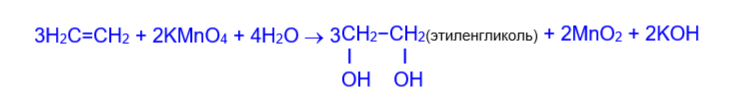
В результате реакции наблюдается обесцвечивание раствора перманганата калия. Реакция Вагнера служит качественной пробой на двойную связь.
7) Полимеризация.
Реакция полимеризации
“Одной из наиболее важных в практическом отношении реакций непредельных соединений (или олефинов) является полимеризация. Реакцией полимеризации называется процесс образования высокомолекулярного соединения (полимера) путем соединения друг с другом молекул исходного низкомолекулярного соединения (мономера). При полимеризации двойные связи в молекулах исходного непредельного соединения «раскрываются», и за счет образующихся свободных валентностей эти молекулы соединяются друг с другом.
Полимеризация олефинов вызывается нагреванием, давлением, облучением, действием свободных радикалов или катализаторов. В упрощенном виде такую реакцию на примере этилена можно представить следующим образом:
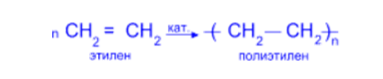
В зависимости от механизма реакции полимеризация бывает двух видов:
1) радикальная, или инициированная и
2) ионная, или каталитическая.”
Радикальная полимеризация
“Радикальная полимеризация вызывается (инициируется) веществами, способными в условиях проведения реакции распадаться на свободные радикалы — например, пероксидами, а также действием тепла и света.
Рассмотрим механизм радикальной полимеризации.

На начальной стадии радикал-инициатор атакует молекулу этилена, вызывая при этом гомолитическое расщепление двойной связи, присоединяется к одному из атомов углерода и образует новый радикал. Образующийся радикал атакует далее следующую молекулу этилена и по указанному пути приводит к новому радикалу, вызывающему дальнейшие аналогичные превращения исходного соединения.
Как видно, растущая частица полимера вплоть до момента стабилизации представляет собой свободный радикал. Радикал-инициатор входит в состав молекулы полимера, образуя его конечную группу.
Элементная ячейка полиэтилена представляется следующим образом:

Обрыв цепи происходит либо при столкновении с молекулой регулятора роста цепи (им может быть специально добавленное вещество, легко отдающее атом водорода или галогена), либо путем взаимного насыщения свободных валентностей двух растущих полимерных цепей с образованием одной полимерной молекулы.”
Ионная или каталитическая полимеризация
”Ионная полимеризация происходит благодаря образованию из молекул мономера реакцинноспособных ионов. Именно от названия растущей частицы полимера в процессе реакции происходят названия полимеризации — катионная и анионная.
Ионная полимеризация (катионная)
Катализаторами катионной полимеризации являются кислоты, хлориды алюминия, бора и т.д. Катализатор обычно регенерируется и не входит в состав полимера.
Механизм катионной полимеризации этилена в присутствии кислоты как катализатора можно представить следующим образом.

Протон атакует молекулу этилена, вызывая разрыв двойной связи, присоединяется к одному из атомов углерода и образует карбониевый катион или карбкатион.
Представленный тип распада ковалентной связи называется гетеролитическим расщеплением ( с греческого heteros — иной, разный).
Образующийся карбкатион атакует далее следующую молекулу этилена и аналогичным образом приводит к новому карбкатиону, вызывающему дальнейшие превращения исходного соединения.
Как видно, растущей частицей полимера является карбкатион.
Элементная ячейка полиэтилена представляется следующим образом:

Обрыв цепи может произойти вследствие захвата растущим катионом соответствующего аниона или с потерей протона и образованием конечной двойной связи.
Ионная полимеризация (анионная)
Катализаторами анионной полимеризации являются некоторые металлорганические соединения, амиды щелочных металлов и т.д.
Механизм анионной полимеризации этилена под влиянием металлалкилов представляется следующим образом.
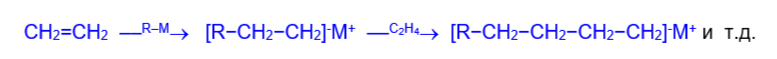
Металлалкил атакует молекулу этилена и под ее воздействием осуществляется диссоциация металлалкила на катион металла и алкил-анион. Образующийся алкил-анион, вызывая гетеролитическое расщепление p- связи в молекуле этилена, присоединяется к одному из атомов углерода и дает новый карбониевый анион или карбанион, стабилизирующийся катионом металла. Образующийся карбанион атакует следующую молекулу этилена и по указанному пути приводит к новому карбаниону, вызывающему дальнейшие аналогичные превращения исходного соединения в полимерный продукт с заданной степенью полимеризации, т.е. с заданным числом мономерных звеньев.
Растущая частица полимера, как видно, представляет собой карбанион.
Элементная ячейка полиэтилена представляется следующим образом:
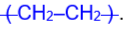
Применение
Алкены широко используются в промышленности в качестве исходных веществ для получения растворителей (спирты, дихлорэтан, эфиры гликолей и пр.), полимеров (полиэтилен, поливинилхлорид, полиизобутилен и др.), а также многих других важнейших продуктов.
Задачи:
- Напишите структурные формулы следующих алкенов: а) 3-метилпентен-2; б) 4,4-диметил-3-этилгексен-1; в) 4-изопропилгептен-2.
- Назовите по заместительной номенклатуре следующие соединения:
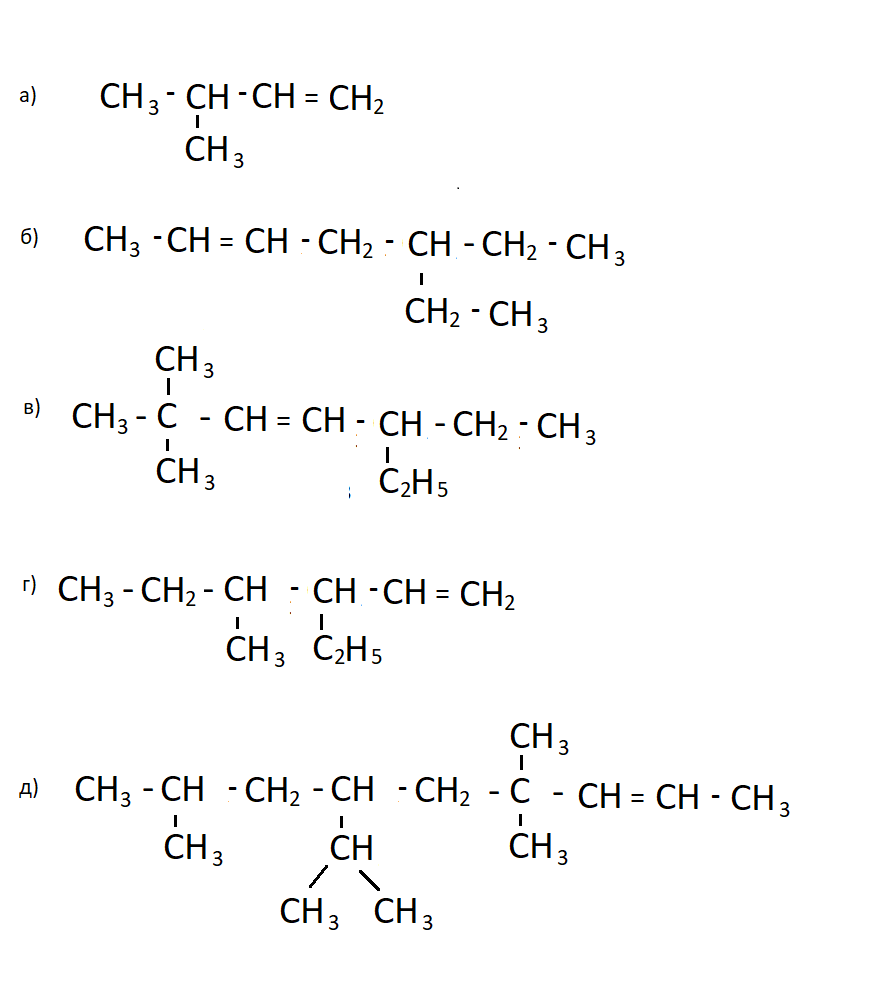
3. Напишите формулы изомерных углеводородов, состав которых отвечает эмпирической формуле С5Н10 Сколько может быть таких углеводородов?
4. Сколько изомерных алкенов соответствует формуле С6Н12? Изобразите их структурные формулы и назовите по заместительной номенклатуре.